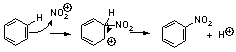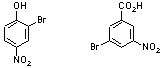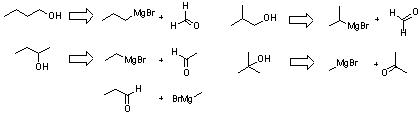|
このページは、2019年3月に保存されたアーカイブです。最新の内容ではない場合がありますのでご注意ください
|
 「ビギナーズ有機化学」 練習問題解答例
「ビギナーズ有機化学」 練習問題解答例
2000.10.8作成
2001.4.6修正
2005.6.29修正
Wordファイル(lha圧縮版、634K)は→
こちら
Acrobatファイル(pdf、125K)は→
こちら
第1章
1.1
Li+ B Mg Al3+ S2- Cl- Ca
陽子数: 3 5 12 13 16 17 20
電子数: 2 5 12 10 18 18 20
1.2
S2-, Cl-, K+, Ca2+
1.3
s軌道電子:1種類のみで、対称な球形の電子分布をもつ。
p軌道電子:3種類あり、互いに直交する方向性をもった電子分布をもつ。
1.4
イオン結合:カチオンの正電荷とアニオンの負電荷の間の静電引力による結合。
共有結合:2つの原子が電子を1個ずつ出し合い、2個の電子を両側の原子が共有することによる結合。
配位結合:一方の原子が2個の電子を相手の原子にあたえてつくる結合。
1.5
炭素は電気的に中性で、電子の偏りのない共有結合をつくり、原子間の電気的反発が少ないため。
1.6
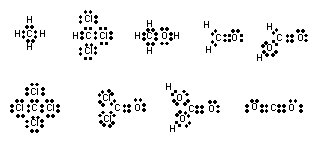
1.7
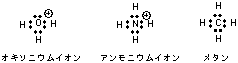
オキソニウムイオンは水の酸素原子のローンペアに水素イオンが配位結合してできたカチオンで、アンモニアとアンモニウムイオンの関係と同じである。
1.8
酸:電子対の受容体。
塩基:電子対の供与体。
第2章
2.1
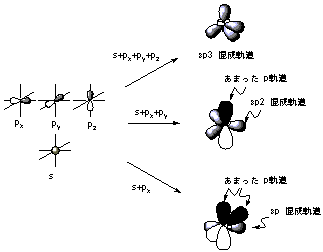
sp3混成軌道はs+px+py+pzの4電子、sp2混成軌道はs+px+pyの3電子、sp混成軌道はs+pxの2電子による混成軌道である。
2.2
p軌道電子は互いに直交する3種類があり、そのうち2個がエチレンの炭素のsp2混成軌道に使われている。sp2炭素のσ結合はこの2個のp軌道電子で決定される平面方向に延びており、残ったp電子でつくられるπ結合はこの平面に直交する方向に立つことになる。
2.3
σ結合は結合の方向と電子の軌道の方向が一致しており、軌道の重なりが大きいのに対し、π結合は軌道の向きと結合方向が直交しており、軌道の重なりが弱いため。
2.4
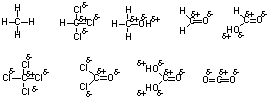
2.5
エタノールのヒドロキシ基のO-H結合は分極しており、水のように分子間で水素結合を形成することができるのに対し、ジメチルエーテルではこのような寄与がないため。
2.6
酢酸イオンの2つのC-O結合は形式的には一方が二重結合、他方が単結合であるが、実際には共鳴によって電子が非局在化しており、完全に対称な構造をとっているため。
2.7
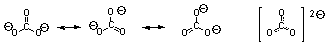
2.8
1,3-ブタジエンでは2個のエチレンユニットのπ結合が平行に配置することによって共役安定化している。エチレンユニットの炭素、水素はπ結合と直交する平面上にあるため、すべての炭素、水素は同一平面上に配置することになる。
第3章
3.1
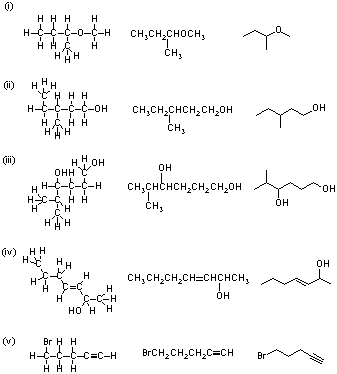
3.2
i)C9H20ii)C7H8 iii)C6H12O5 iv)C6H10O2 v)C15H22O
3.3
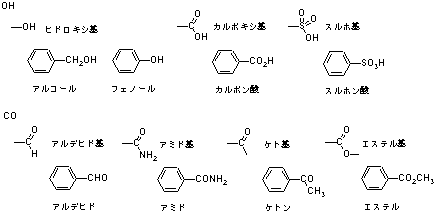
3.4
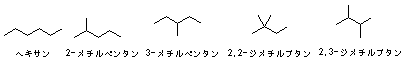
3.5
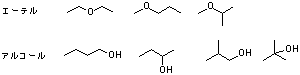
3.6
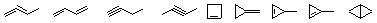
3.7
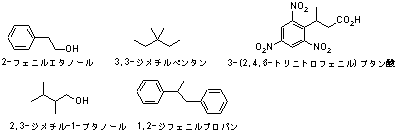
3.8
IUPAC命名法では最も長い炭素鎖を基本骨格として命名するので、枝分れのある炭化水素では全炭素数よりも短い炭化水素が骨格となるため。
第4章
4.1
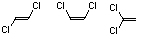
4.2
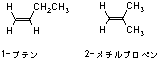
1-ブテンや2-メチルプロペンでは、二重結合の片方の炭素に結合している置換基が同一であり、他方の炭素上の置換基との相対的位置関係に差が出ないため。
4.3
2-ブテンのシス-トランス異性化反応はπ結合の切断再結合、1,2-ジメチルシクロペンタンのそれはσ結合の切断再結合が必要であり、強い結合であるσ結合の方が切れにくいため。
4.4
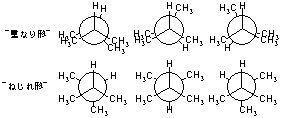
4.5
安定なコンホメーションでは、すべての炭素-炭素結合についてブタンのC2-C3間のように最安定なアンチ形をとるのでジグザグ形になる。
4.6
シクロヘキサンはいす形コンホメーションをとることによってすべての炭素間結合がねじれ形に配置し、結合角がひずみのない109°の角度をとることができるため。
4.7
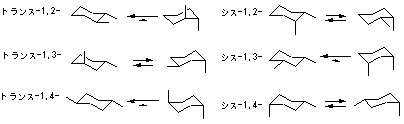
4.8
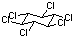
第5章
5.1
キラル:グローブ、ゴルフクラブ、ハサミ、ネジ、ワイシャツ、など。
アキラル:バット、ボール、鉛筆、クギ、Tシャツ、など。
5.2
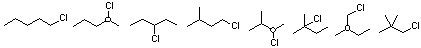
5.3
+/−、d/l:平面偏光を右に回転させるもの(+,d)と左に回転させるもの(-,l)。
D/L:右旋性のグリセルアルデヒドに対応する置換基配置のもの(D)とその鏡像体(L)。
R/S:順位則により最低順位置換基の裏側から分子を見たときに他の3置換基の配置を高順位のものからたどって時計回りのもの(R)と反時計回りのもの(S)。
5.4
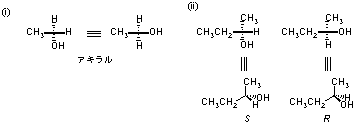
5.5
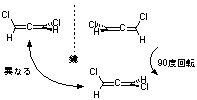
5.6
(R)-乳酸と(R)-アミンの塩は(R,R) 体、(S)-乳酸と(R)-アミンの塩は(S,R) 体となり、両者はジアステレオマーの関係にあるので、溶解度等の物理的性質が異なるため容易に分離できる。
5.7
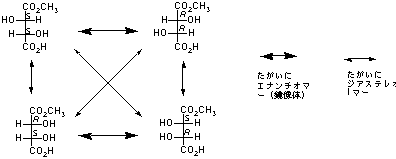
5.8
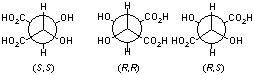
第6章
6.1
古典的には一群のベンゼン誘導体のように芳香を有すること、現在では環状共鳴構造をもちヒュッケル則により安定化しうること。
6.2
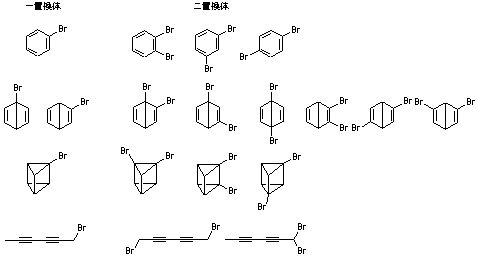
6.3
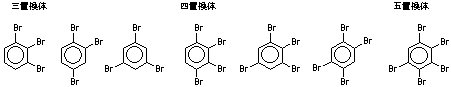
6.4
ケクレ構造は六角形に二重結合が3個はいり、その位置がきわめて速く連続的に移動している構造。環状共鳴構造は6個のπ電子が環状に一様につながった構造。
6.5
ベンゼンの各炭素間には通常のσ結合の他にπ電子6個からなるπ結合が存在するが、環状共鳴構造により6本の結合上に6個の電子が一様に分布している。そのため結合1ヶ所あたり0.5本分となり、σ結合とあわせて1.5本分、すなわち二重結合よりは弱く単結合より強い。
6.6
ベンゼンは形式的にはシクロヘキサンに二重結合が3個はいって構造であるが、環状共鳴構造により大きくエネルギーが低下しているため。
6.7
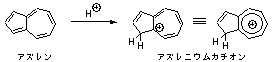
6.8
ピロールの窒素のローンペアは環状共鳴構造に組み込まれているため、他の原子に塩基として供与することができにくいが、イミダゾールでは2個の窒素のうち1個のローンペアは環状共鳴構造に参加していないため塩基性を示しうる。
第7章
7.1
ラジカル反応は1電子移動、イオン反応は2電子移動による結合の切断、生成をともなう反応。
7.2
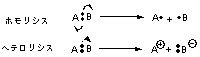
7.3
求電子反応は電子不足化学種が電子対を求めて反応が起きる。すなわちルイス酸がルイス塩基を攻撃する。
求核反応は電子豊富化学種が電子不足種を求めて反応が起きる。すなわちルイス塩基がルイス酸を攻撃する。
(2001.4.6修正)
7.4
出発物から生成物へのエネルギー変化のうち、途中に通る過渡的なエネルギー極大状態を遷移状態、そこに達するのに必要なエネルギーを活性化エネルギーという。
活性化エネルギーの山を2回越す二段階反応において、活性化エネルギーが大きい方の段階を律速段階、2つの遷移状態にはさまれたエネルギー極小の準安定状態を中間体という。
7.5
発熱反応は出発物と生成物の間の熱収支は発熱になるが、途中で高エネルギーの遷移状態を経ねばならないため、加熱によって反応速度が増大する。
7.6
濃度:反応チャンス(反応分子の出会い)が変化する。
温度:活性化エネルギーを越えるに足る潜在エネルギーをもつ分子数が変化する。
触媒:より活性化エネルギーの小さい別経路の反応をあたえる。
7.7
一分子反応、すなわち反応物が他の影響を受けずに自発的に分解する段階が律速段階になっている反応。
7.8
速度論生成物を得るにはより反応が平衡状態に達しないようにより低い温度でおだやかに反応を行ない、熱力学生成物を得るには十分にエネルギーを与えた状態で反応を行なう。
第8章
8.1
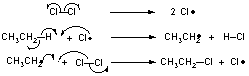
8.2
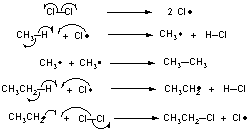
8.3
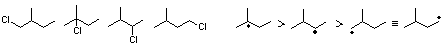
8.4
塩素(塩素分子のホモリシスが律速段階)。
8.5
臭素化反応は吸熱反応であるため。
8.6
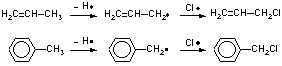
8.7
ラジカルが共鳴によって3個のベンゼン環に均等に非局在化できるため。
8.8
リノール酸の11位のメチレンは両側を二重結合にはさまれているため安定なラジカルとなりうるが、オレイン酸は二重結合が1個のみであり、このような安定ラジカルができないため。
第9章
9.1
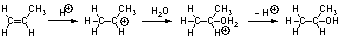
1段階目の水素イオンの付加反応が律速段階なため。
9.2
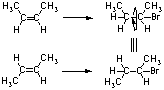
9.3
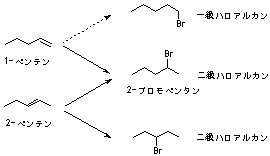
9.4
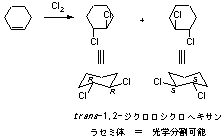
9.5
中間に生成した環状ブロモニウムカチオンを水分子が攻撃して開環反応を起こした。
9.6
アセチレンに1分子目の塩化水素が付加して生成したクロロエチレンは非対称アルケンであるため、マルコフニコフ則により水素の多い側の炭素にさらに水素が付加したため。
9.7
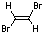
9.8
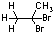
第10章
10.1
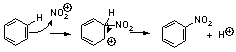
10.2
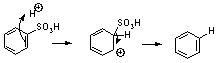
10.3
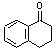
10.4
フェノールのヒドロキシ基はオルト-パラ配向性基であると同時に電子供与性のベンゼン環活性化基であるため、強い条件のニトロ化反応ではすべてのオルト、パラ位に置換反応が進行するため。
10.5
オルト-パラ配向性:-NHCOCH3、-OCH3、 メタ配向性:-COCH3、-N+(CH3)3、-CF3。
10.6
アミノ基の窒素上のローンペアの共鳴効果によるベンゼン環への電子供給力が、メチル基の電子を押し出す力よりはるかに強いため。
10.7
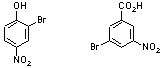
10.8
2001.5.24リンク誤り修正(オンライン版のみ)
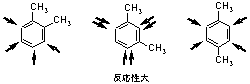
第11章
11.1
SN2反応は脱離するハロゲンの裏側から求核試剤の攻撃が起きるため、攻撃される炭素に結合している残り3個の置換基の立体障害が大きく反応性を左右する。このため立体的に小さい水素を多くもつ級数の低いハロゲン化物が有利になる。
SN1反応では、ハロゲン化物イオンの脱離によるカルボカチオン生成が律速段階であるため、安定なカルボカチオンすなわち級数の高いカルボカチオンを生成しうるハロゲン化物が有利になる。
11.2
SN1反応はカルボカチオン中間体を経るため、より安定なカチオンに変化しうる場合は、骨格転位を起こす余地があるが、SN2反応は求核試剤の攻撃とハロゲンの脱離が同時に進行し、カチオン中間体を経由しないため転位反応は起こらない。
11.3
キラルな出発物質を用いれば、そのキラリティが生成物では反転していることを旋光性で確かめることができる。
11.4
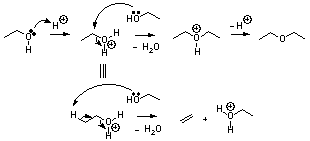
11.5
ハロゲンの結合している炭素がベンゼン環のsp2炭素であり、電子を豊富にもっているため。
11.6
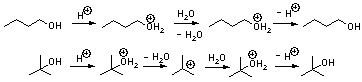
いずれも過剰の重酸素水と酸触媒を用いて求核置換反応を起こさせればよい。反応系は平衡状態になるので、用いたアルコールと重酸素水のモル比に応じた生成物が得られる。
11.7
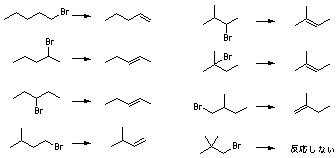
11.8
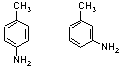
第12章
12.1
アルキル基の電子供与性が炭素の負電荷を強めるので安定性は逆になる。
12.2
カルボニルの炭素-酸素間二重結合は酸素の電気陰性度の高さのために分極しており、相対的に炭素の電子密度が下がっているため。
12.3
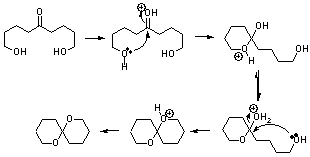
12.4
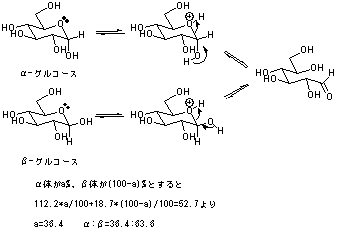
12.5
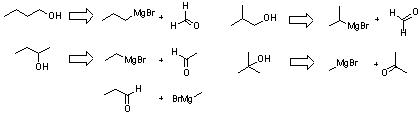
12.6
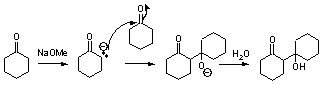
12.7
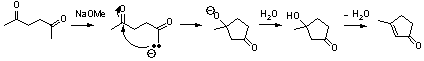
12.8
マロン酸エステルは2つのカルボキシ基にはさまれたメチレンをもち、その水素が塩基によって引き抜かれてできるエノラートアニオンは両側のカルボニルと共鳴することができるため安定で生成しやすいため。
|
このページは、2019年3月に保存されたアーカイブです。最新の内容ではない場合がありますのでご注意ください
|
![]() 「ビギナーズ有機化学」 練習問題解答例
「ビギナーズ有機化学」 練習問題解答例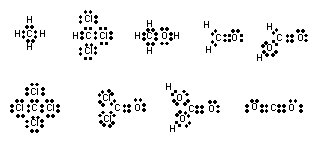


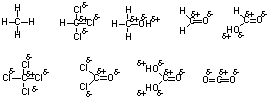
![]()
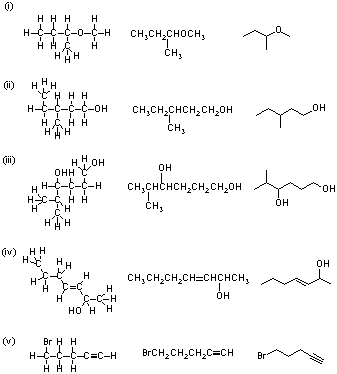

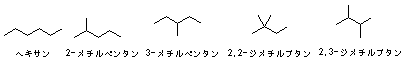

![]()

![]()
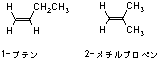
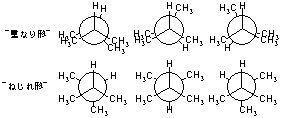
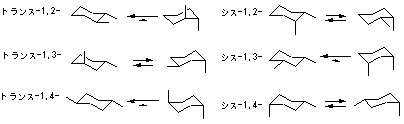
![]()
![]()
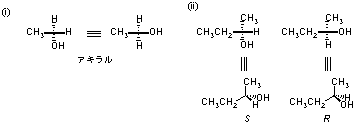


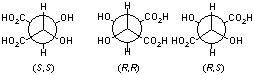


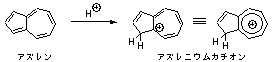
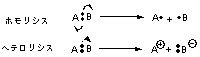
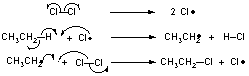
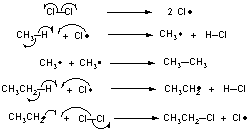
![]()
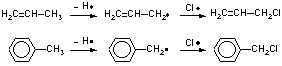
![]()
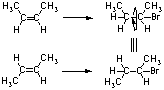

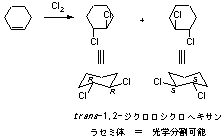
![]()
![]()