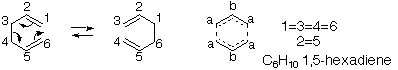
| このページは、2019年3月に保存されたアーカイブです。最新の内容ではない場合がありますのでご注意ください |
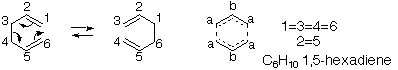
で、この反応が可逆的に速く進行すると、出発物と生成物は平衡になって区別できなくなります。すなわちC-1,C-3,C-4,C-6は
等価
になります。
NMR
では炭素も水素も2種類(C-1,3,4,6の組とC-2,5の組)しかなくなってしまうわけです。
ここまででもなかなか面白いんですが、次にヘキサジエンの開いた端(C-1,C-6間)を
メチレン
で橋架けして結んだ形を考えてみます。左右対称でないと等価になりませんから、同時にC-3,C-4間にも同じ橋架けをしておきます。できた分子が次の
ホモ
トロピリデンです。図のC-4とC-8が新しく付加されたメチレンで全体はC8H10となります。
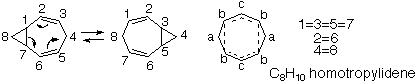
この分子も同じように速い速度でCope転位を起こして平衡になると、C-1,C-3,C-5,C-7が等価になります。
次に三次元展開をします(^^;。ホモトロピリデンの構造をよく見ると、
シクロプロパン
環の三角形の2個の炭素と反対端の炭素を2本のエチレン鎖(−CH=CH−)でつないだ形であることにお気づきでしょうか。三角形の残った炭素と端の炭素をもうひとつのエチレン鎖でつないでやれば、
三回対称
のかご型の立体分子になります。それがブルバレンです。
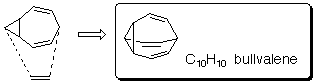
このブルバレンが同じようにCope転位反応をするとどうなるでしょう。番号をふって考えてみると、ホモトロピリデンのときと同じにC-1,C-7間が切断し、同時にC-3,C-5間に結合が生成すると図の右側の構造になります。
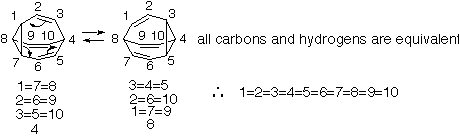
ここで、分子は三回対称構造ですから、各炭素(水素)の等価性をみてみると、末端の炭素以外はそれぞれ3個ずつの等価な組にわかれます。転位反応が十分速く進行し、出発構造と生成構造間が区別できなくなれば、両側の構造の等式が同時に成り立つことになりますから、結局、すべての炭素が等号で結ばれてしまいました(^^)。これはブルバレンC10H10のすべての炭素、すべての水素は等価であるということを表しています。事実、1H-NMRスペクトルでは十分温度が高ければ(100℃)、δ4.2ppmにシグナルが1本しか観測されないことがわかっています。
なんかだまされたみたいに不思議な話ですね。ブルバレンは分子が対称なために、常に起こりうるCope転位反応が三通り存在し、それが等しい確率で起きます。最初の図でいうと上記のほか、C-1,C-8切断、C-3,C-10形成の反応と、C-7,C-8切断、C-5,C-10形成の反応が同時に起こります。それぞれの生成物もやはり三通りの転位を起こしますから、つまりホモトロピリデンのような単純に両側の構造をいったりきたりではなく、結合の切断形成が複雑に連なってどんどん新しい構造(といっても分子自体は常に同じブルバレンなわけですが(^^;)に変換されていくために、結局すべてが等価になってしまうのです。
ref. G. Schroeder,Angew.Chem.Int.Ed.Engl.,2, 481 (1963)
ほんと、おもしろ化合物っておもしろいですね(笑)。
| このページは、2019年3月に保存されたアーカイブです。最新の内容ではない場合がありますのでご注意ください |