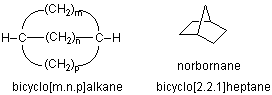
| このページは、2019年3月に保存されたアーカイブです。最新の内容ではない場合がありますのでご注意ください |
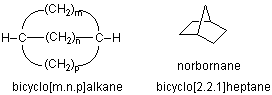
ところで、似たような分子にプロペランとかパドランとかいうのもあって、それぞれビシクロアルカンのメチン間を単結合でつないだプロペラ形の分子と、メチレン鎖でつないだ水車型(外輪船の回転輪がパドル)の分子です。こういう分子もなかなかにおもしろいのですが、それはまたの機会のお楽しみということにして、今回はシンプルなビシクロアルカンに話をもどしましょう。
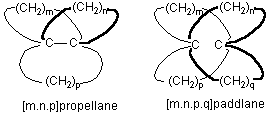
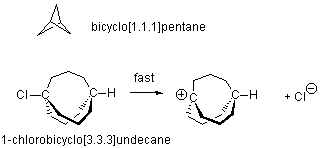
さて、ビシクロアルカンのうち対称構造をもつm=n=pの炭化水素を考えます。このうち最小の分子は、ビシクロ[1.1.1]ペンタンで、すべての環がひずみの大きいシクロブタン環からなっているので大変不安定な分子です。このメチン炭素間の 非結合距離 は、0.189 nm とのことです。普通のCC結合距離が0.154nm、それが分子によっては0.17nmていどまで延びているものがあるそうですから、このビシクロ[1.1.1]ペンタンのメチン間距離は非結合炭素間としては相当近いですね。もちろん3個のメチレンでひきつけられている効果でしょう。
これは極端な
小員環
の例ではありますが、逆に環を拡大していくとやはり分子にはひずみがかかります。橋頭炭素間のメチレン鎖を3にしたのがビシクロ[3.3.3]ウンデカンで、これくらいになると余裕がありそうですが...。このメチン水素を塩素で置換した1-クロロ体は、塩化t-ブチルなど他の
三級
ハロゲン化物に比べて容易に
ソルボリシス
反応を受けて、
カルボカチオン
を生成することが知られています。これは
正四面体形
の
sp3
炭素がカルボカチオンになると平面三配位になるためで、つまり橋頭位炭素が平面になることで分子全体のひずみが解消されるために、塩化物イオンの脱離が容易に進行するというわけです。
ここからが本題なのですが(^^;、ならばもっとメチレン鎖を長くしてやったらどうでしょう。メチレン3個ていどでも通常のsp3形よりも平面の方が安定になるならば、もっと長くすれば橋頭位炭素の配置がひっくりかえって水素が内側を向いた形が安定になるのではないでしょうか。え、想像できないって? 次の図を見てください。
これはm=n=p=8のビシクロ[8.8.8]ヘキサコサンです。これくらいになると橋頭位炭素が逆の配置のものができるようになります。これまでのビシクロアルカンのように橋頭位水素が外に突き出ているのを“out,out”異性体とすると、片側の炭素がひっくり返って水素が内側へ向いた“out,in”、両方ともひっくり返った“in,in”の異性体が考えられます。それぞれの分子をクリックすると立体構造が表示できます(表示に少し時間がかかります。表示にはChimeプラグインが必要です。ダウンロードの説明は→
こちら
、マニュアルは→
こちら
)
実際にこういう異性体が作り分けられているというのが驚きです。どうやって合成するかというと、まず環状ジケトン、シクロオクタデカン-1,10-ジオンからスタートして、
グリニャール反応
で炭素鎖を導入します。このとき環に対して2つの
アルキル鎖
が
シス
配向のものと
トランス
配向のものができます。炭素鎖を数段階の工程で
増炭
したジエステルに変換しますが、その途中でこのシスとトランス異性体を分離することができます。シスとトランスの区別は、アルキル基がC3の段階では両端の分子内
閉環
反応をするとシス形しか閉環できないことからわかりました。
最後に、ジエステルを分子内
アシロイン縮合
するとシス体のみならずトランス体も閉環体を与えます。還元してメチレンにしてやってできあがりです。
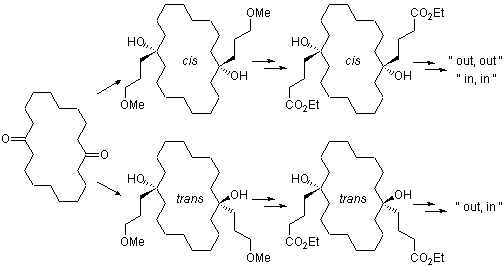
この場合、シス体からは“out,out”と“in,in”、トランス体からは“out,in”異性体が生成するはずですが、実際にはシス体の閉環体は“in,in”のみで、“out,out”は生成しませんでした。おそらく水素が外を向いた形はひずみが大きいのでしょう。生成したのが“in,in”であるということは、三級水素の
イオン反応
による臭素化を行なっても反応しないこと(“out,in”は反応する)や計算化学的根拠から推定されています。
環が大きくなると、両端が外向きの水戸納豆のような引き伸ばされた形よりは、内向きの丸っこい俵形のほうが分子内の非結合相互作用が小さくて安定なのでしょう。「鬼は外・福は内」というわけです(ちょっと苦しいか(^^;)。
ref. C.H. Park and H.E.Simmons,J.Am.Chem.Soc.,94, 7184 (1972)
| このページは、2019年3月に保存されたアーカイブです。最新の内容ではない場合がありますのでご注意ください |