| このページは、2019年3月に保存されたアーカイブです。最新の内容ではない場合がありますのでご注意ください |
<四角酸が強いわけ>
分子やイオンは
共鳴
によって安定化する。共鳴構造が電子の移動によって次々にたくさん書ければ、それだけ電荷の分散が大きくなるため、より安定になる。酢酸イオンの場合は2種類の
極限構造
だけだったが、環状につながって電子の移動が連続的に起こるようなイオンが存在する。

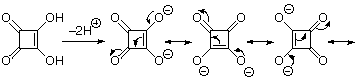
たとえば、通称「四角酸」とよばれる図の酸は、水素イオン2個を放出して2価イオンになると、連続的な電子移動により、電荷が各頂点の酸素上に分散されて、非常に安定な アニオン となる。そのため、四角酸は有機化合物でありながら硫酸に匹敵する強い酸性を示す。同じような同族体に、三角形から七角形の酸が知られている( おもしろ化合物第7話 参照)。
| このページは、2019年3月に保存されたアーカイブです。最新の内容ではない場合がありますのでご注意ください |